3 Газовые смеси
3.11 Определить газовую постоянную, плотность при нормальных условиях и объемный состав смеси, если: H2=8,4%; CH4=48,7%; C2H4=6,9%; CO=17%; O2=4,7%; N2=6,7%
Ответ: Rсм=717 Дж/(кг·К), rH2=0,484, rCH4=0,351, rC2H4=0,028, rCO=0,072, rCO2=0,02, rO2=0,017, rN2=0,028, ρн=0,518 кг/м³.
Скачать файл (банки РФ) 150 RUBВсе задачи из: Рабинович О.М. Сборник задач по технической термодинамике
3.12 Найти газовую постоянную, удельный объем газовой смеси и парциальные давления ее составляющих, если объемный состав смеси следующий: CO2=12%; CO=1%; H2O=6%; O2=7%; N2=74%, а общее давление ее р=100 кПа.
Ответ: Rсм=281 Дж/(кг·К), υсм=0,76 м³/кг, рСО2=12 кПа, рСО=1 кПа, рН2О=6 кПа, рО2=7 кПа, рN2=74 кПа.
Скачать файл (банки РФ) 130 RUBВсе задачи из: Рабинович О.М. Сборник задач по технической термодинамике
3.13 Массовый состав смеси следующий: CO2=18 %; O2=12 % и N2=70 %. До какого давления нужно сжать эту смесь, чтобы при t=180ºC 8 кг ее занимали объем, равный 4 м³.
Ответ: р=0,24 МПа.
Скачать файл (банки РФ) 120 RUBВсе задачи из: Рабинович О.М. Сборник задач по технической термодинамике
3.14 Определить массовый состав газовой смеси, состоящей из углекислого газа и азота, если известно, что парциальное давление углекислого газа рСО2=120 кПа, а давление смеси рсм=300 кПа.
Ответ: mCO2=0,512, mN2=0,488.
Скачать файл (банки РФ) 120 RUBВсе задачи из: Рабинович О.М. Сборник задач по технической термодинамике
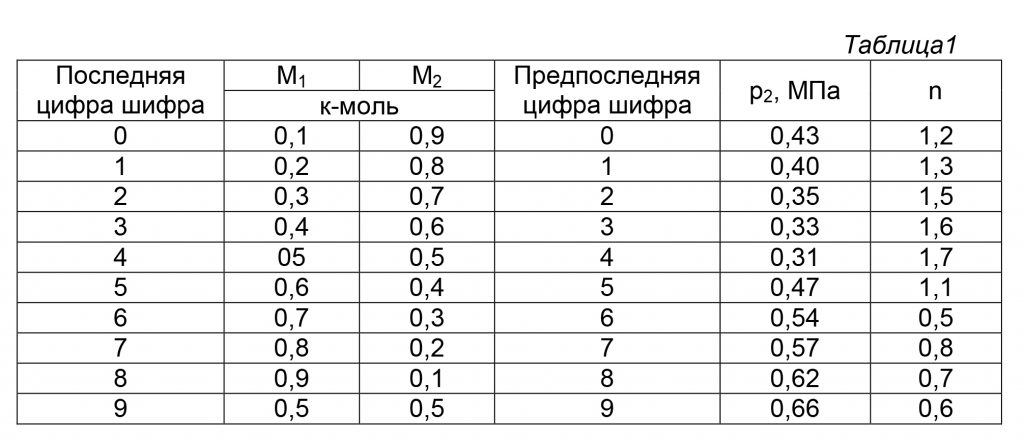
3.15 Смесь, состоящая из М1 киломолей азота и М2 киломолей кислорода с начальными параметрами р1 = 1 МПа и Т1 = 1000 К, расширяется до давления р2. Расширение может осуществляться по изотерме, адиабате и политропе с показателем n. Определить газовую постоянную смеси, ее массу и начальный объем, конечные параметры смеси, работу расширения и теплоту, участвующую в процессе.
Дать сводную таблицу результатов и анализ ее. Показать процессы в рυ и Ts — диаграммах. Данные необходимые для решения задачи, выбрать из таблицы 1.
Указание. Показатель адиабаты, а следовательно, и теплоемкости cр и сυ следует принять постоянным, не зависящим от температуры.
Выбрать вариант задачи
ВУЗ: КГУ
Все задачи из: Савельев В.А. Техническая термодинамика КГУ Курган 2020
3.16 Смесь, состоящая из М1 киломолей азота и М2 киломолей кислорода с начальными параметрами р1=1 МПа и Т1=1000 К, расширяется до давления р2. Расширение может осуществляться по изотерме, адиабате и политропе с показателем n. Определить газовую постоянную смеси, ее массу и начальный объем, конечные параметры смеси, работу расширения, теплоту, участвующую в процессе, изменение внутренней энергии, энтальпии и энтропии. Дать сводную таблицу результатов и анализ ее. Показать процессы в pυ и Ts — диаграммах. Данные необходимые для решения задачи, выбрать из табл. 26.
Таблица 26
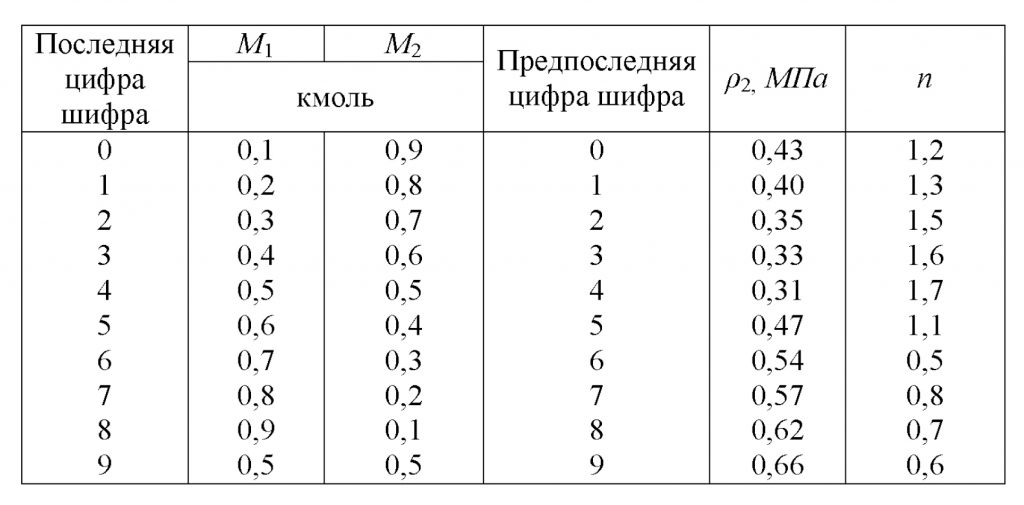
Указание. Показатель адиабаты, а следовательно, и теплоемкости ср и сυ следует принять постоянным, не зависящим от температуры
Ответить на вопрос: как зависит работа расширения от показателя политропы n и почему?
Выбрать вариант задачи
ВУЗ: ТОГУ
3.17 Расчет газовой смеси
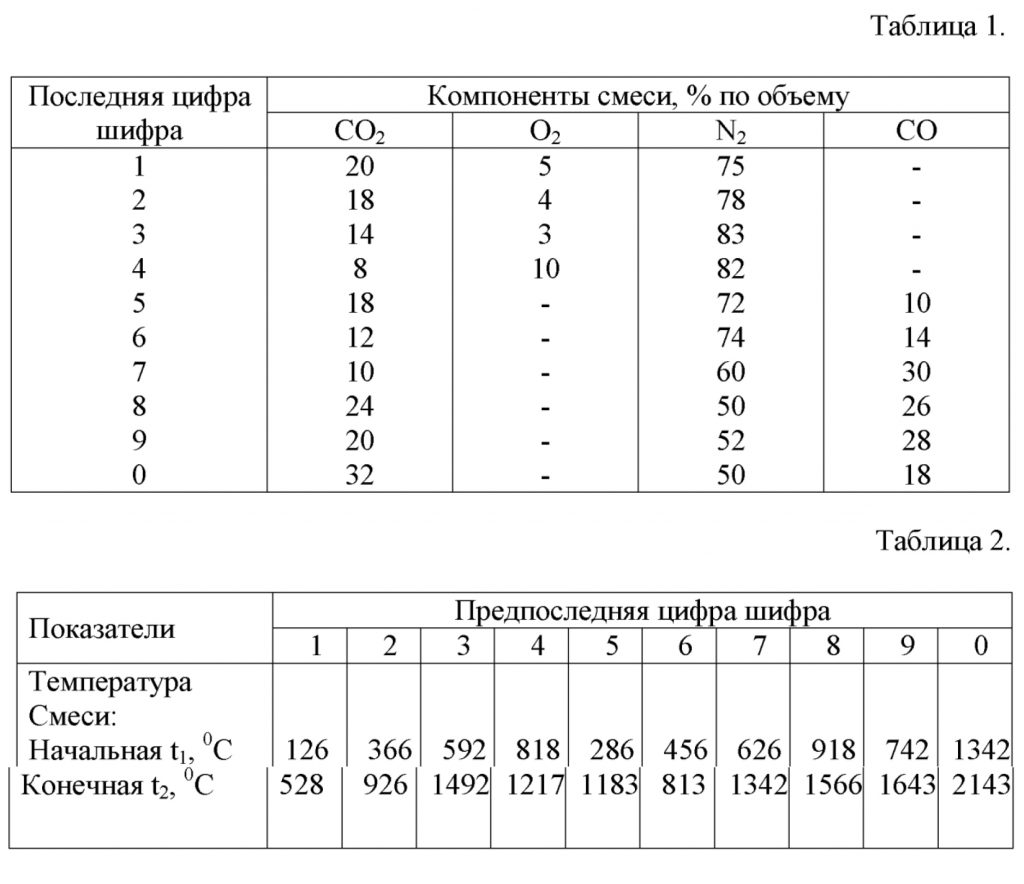
Газовая смесь состоит из нескольких компонентов, содержание которых в смеси задано в процентах по объему (табл.1.1).
Определить:
1) кажущуюся молекулярную массу смеси;
2) газовую постоянную смеси;
3) средние мольную, объемную и массовую теплоемкости смеси при постоянном давлении в пределах температур от t1 до t2 (табл.1.2).
1. Что называется удельной газовой постоянной? Единица ее измерения в системе СИ. Чем она отличается от универсальной газовой постоянной?
2. Что представляют собой массовая, объемная и мольная теплоемкости. Каковы единицы их измерения в системе СИ. Какова связь между указанными теплоемкостями.
3. Какие факторы влияют на величину теплоемкости.
Выбрать вариант задачи
Методичка: Техническая термодинамика.pdf
Методичка: Техническая термодинамика и теплопередача.pdf
ВУЗ: ТОГУ
3.18 Найти газовую постоянную, удельный объем газовой смеси и парциальные давления ее составляющих, если объемный состав смеси следующий: CO2=12%; CO=1%; H2O=6%; O2=7%; N2=74%, а общее давление ее составляет 750 мм рт. ст.
Скачать файл (банки РФ) 130 RUB3.19 Газовая смесь массой m, имеющая начальную плотность 0,9 м³/кг, в ходе политропного процесса сжимается от давления 0,1 МПа до давления рк. При этом её температура достигает значения Тк.
Определить:
— удельную газовую постоянную смеси;
— показатель политропы сжатия;
— подводимую теплоту, изменение внутренней энергии и энтальпии, а также работу, совершенную газом;
— изобразить процесс сжатия на обобщенных p-υ и T-s диаграммах.
Принимаемые допущения:
— температурной зависимостью теплоемкости пренебречь;
— смесь считать идеальным двухатомным газом;
— контроль вычислений энергетических характеристик процесса выполнить по первому закону термодинамики.
Данные для расчета выбрать из таблицы 1.
Таблица 1
| Вариант | m, кг | рк, кПа | Состав смеси | tk, ºC | |||
| доли | Н2 | N2 | O2 | ||||
| 00 | 0,3 | 465 | массовые | 0,06 | 0,1 | 0,84 | 115 |
Варианты задачи: 01, 11, 12, 13, 16, 21, 22, 24, 33, 34, 36, 37, 41, 44, 50, 56, 61, 64, 74, 84, 86, 87, 88.
ВУЗ: ПГТУ
3.20 Состав газовой смеси, представляющей собой продукты сгорания топлива, задан (табл.1) объемными долями компонентов в процентах.
Определить:
1 Молекулярную массу и газовую постоянную смеси.
2 Удельный объем и плотность смеси при нормальных условиях.
3 Среднюю мольную, массовую и объемную теплоемкости смеси при постоянном давлении в интервале температур от 0 до t1,ºC и от 0 до t2,ºC.
4 Энтальпию 1 смеси при температуре t1 и t2,ºC.
5 Теплоту, отданную 1 кг смеси при изобарном охлаждении ее от t1 до t2,ºC.
Состав газовой смеси взять из табл.1 по последней цифре шифра, начальную и конечную температуру смеси — по предпоследней.
Таблица 1
| Вариант 68 | |||||
| CO2, % | H2O, % | N2, % | O2, % | t1,ºC | t2,ºC |
| 12,4 | 9,6 | 72,2 | 5,8 | 800 | 300 |









































