4 Теплоемкость газов
4.31 Найти среднюю изохорную молярную теплоемкость продуктов сгорания топлива при их охлаждении от 1100 до 300 ºС. Количества вещества компонентов смеси следующие: углекислый газ — nCO2, кислород — nO2, азот — nN2, водяные пары — nH2O.
Таблица 1 – Исходные данные
| Вариант | nCO2, моль | nO2, моль | nN2, моль | nH2O, моль |
| 9 | 45 | 38 | 270 | 31 |
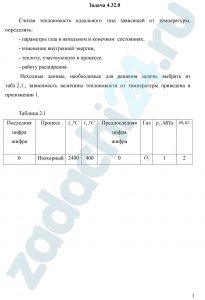
4.32 Считая теплоемкость идеального газа зависящей от температуры, определить: параметры газа в начальном и конечном состояниях, изменение внутренней энергии, теплоту, участвующую в процессе и работу расширения.
Исходные данные, необходимые для решения задачи, выбрать из табл.2,1., зависимость величины теплоемкости от температуры приведена в приложении 1.
Таблица 1
| Вариант | Процесс | t1, °С | t2, °С | Газ | р1, МПа | m, кг |
| 00 | Изохорный | 2400 | 400 | O2 | 1 | 2 |
Варианты задачи: 01, 02, 03, 04, 05, 06, 07, 08, 09, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99.
ВУЗ: ТюмГНГУ
4.33 Вычислить среднюю массовую и среднюю объемную теплоемкость окиси углерода при постоянном объеме для интервала температур 0-1200 ºС, если известно, что для окиси углерода (μсрm)01200=32,192 кДж/(кмоль·К).
Ответ: (μсυm)01200=0,8528 кДж/(кг·К), (с′υm)01200=1,0659 кДж/(м³·К).
Все задачи из: Рабинович О.М. Сборник задач по технической термодинамике
4.34 Вычислить среднюю массовую и среднюю объемную теплоемкость углекислого газа при постоянном объеме для интервала температур 0-800 ºС, если известно, что для окиси углерода (μсрm)8000=47,763 кДж/(кмоль·К)).
4.35 Вычислить среднюю массовую и среднюю объемную теплоемкость воздуха в интервале температур от t1=20 ºC до t2=800 ºC в процессе при постоянном объеме пользуясь таблицами. Сравнить полученные результат со значениями теплоемкостей, подсчитанными по молекулярно – кинетической теории.
4.36 При нагреве некоторого количества газа при определенных условиях (табл. 1.3) температура газа повышается от t1 до t2. Определить количество теплоты, переданное газу в этом процессе, учитывая зависимость теплоемкости от температуры.
Таблица 1.3 — Исходные данные
| Вариант | природа
газа |
условия
нагрева |
t1, ºC | t2, ºC | количество
газа |
| 0 | воздух | постоянный
объем |
0 | 600 | 2 кг |
Варианты задачи: 1, 2, 3, 4, 5, 6, 7, 8, 9.
ВУЗ: ДВГУПС
4.37 Газовая смесь имеет следующий состав по объему: СО=20%, N2=80%. Определить для данной смеси среднюю массовую теплоемкость Сυm в интервале от t1 до t2, если смесь нагревается от t1=80ºС до t2=110ºС.
4.38 Вычислить среднюю массовую и среднюю объемную теплоемкость двуокиси углерода при постоянном объеме в интервале температур от t1, ºС до t2, ºС , считая зависимость теплоемкости от температуры нелинейной. Задачу решить с помощью таблиц нелинейной зависимости теплоемкости от температуры Б1-Б4 (Приложение Б). Данные для расчета приводятся в таблице 1.4.
Таблица 1.4 – Расчетные данные
| Вариант | t1, ºC | t2, ºC |
| 10 | 80 | 540 |
4.39 Найти среднюю объемную теплоемкость сʹpm и сʹυm для воздуха в пределах 400 ÷ 1200 ºС, считая зависимость теплоемкости от температуры нелинейной.
4.40 Продукты сгорания топлива поступают в газоход парового котла при температуре газов tʹг=1100 ºС и покидают газоход при температуре tʺг=700 ºС. Состав газов по объему: rCO2 = 11%; rO2 = 6%; rH2O = 8%; rN2 = 75%.
Определить, какое количество теплоты теряет 1 м³ газовой смеси, взятой при нормальных условиях.
Ответ: Qp=539,2 кДж/м³.
Все задачи из: Рабинович О.М. Сборник задач по технической термодинамике